Под коррозией понимают разрушение металлов или их сплавов в результате взаимодействия с внешней средой. Под влиянием коррозионных процессов состав и свойства металлов изменяются, и, если не принять меры защиты, металлы превращаются в соответствующие окислы или соли. На рис. 1 показана палуба судна, защите которой от коррозии не уделялось требуемого внимания.
Различают два основных вида коррозии: химическую и электрохимическую.
Химическую коррозию вызывают сухие газы, а также различные органические жидкости, неэлектролиты (бензин, керосин, спирт и т. д.), не проводящие электрический ток.
Причиной возникновения электрохимической коррозии могут быть электролиты-—вещества, проводящие электрический ток (морская вода, растворы кислот, щелочей и т. п.), а также влажные газы или тонкая пленка атмосферной влаги. Такая коррозия возникает при взаимодействии металла с электролитом и сопровождается переносом электричества.
Металлические изделия как в процессе эксплуатации, так и при хранении, неизбежно подвергаются коррозии. Скорость и характер коррозионных разрушений металла находится в прямой зависимости от среды, содержания кислорода, температуры и перемещения изделия в электролите. Возникая на поверхности металла, коррозия редко имеет равномерный характер. Как правило, коррозионные разрушения металла носят неравномерный характер или наблюдаются в виде пятен на отдельных участках конструкции. В отдельных случаях коррозия сосредотачивается на очень малой поверхности, вызывая глубокие разрушения в виде язв или точек. Нередки случаи, когда разрушение металла почти, незаметно с поверхности и происходит вдоль границ кристаллов, нарушая связь между ними и вызывая межкристаллитную коррозию. Это самый опасный вид коррозии, сопровождающийся часто полной потерей прочности конструкции. Различают также подповерхностную коррозию, сопровождающуюся вспучиванием или расслаиванием металла.
В судостроении коррозия наружных конструкций вызывается действием электролита на подводную часть корпуса судна, район переменной ватерлинии, частично надводный борт, надстройки, палубы, куда попадают брызги морской воды. Во внутренних помещениях коррозия возникает под влиянием тонкой пленки влаги с растворенными в ней газами и частицами соли, всегда содержащимися в морском воздухе. В результате коррозии поверхность металла становится изъязвленной, шероховатой, цвет его изменяется, изделие теряет механическую прочность.
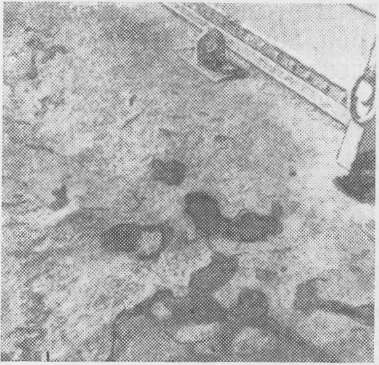
Рис. 1. Коррозия стальной палубы, не имевшей защитного покрытия
При действии электролита металл стремится перейти в раствор. Скорость растворения металлов в электролитах различна.
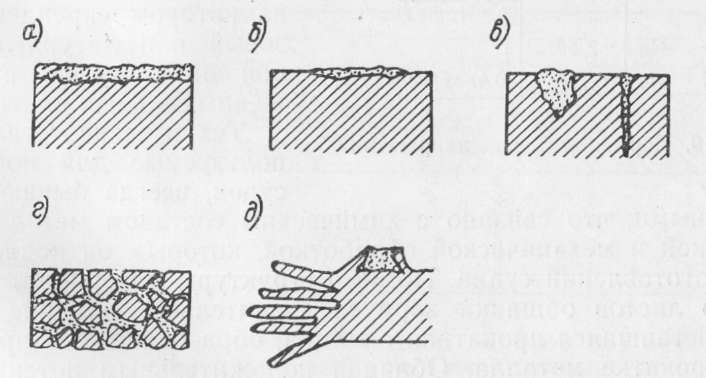
Рис. 2. Виды коррозионных разрушений металла:
а — равномерная; б — в виде пятен на отдельных участках конструкции; в — глубокие разрушения в виде язв; г — межкристаллитная; д — подповерхностная
Одни из них растворяются очень интенсивно и быстро насыщают растворы, другие, даже после длительного соприкосновения с электролитом, растворяются незначительно.
В зависимости от того, как быстро происходит растворение металлов в электролите, т. е. с какой скоростью они способны подвергаться коррозионным разрушениям, металлы располагаются в последовательности, указанной на рис. 10.
В этом ряду металлы, расположенные выше водорода, электроположительны, а ниже — электроотрицательны. Чем более электроотрицателен металл, тем легче он будет переходить в раствор.
Если построить гальванический элемент из двух разнородных металлов, то в таком элементе каждый металл будет
анодом по отношению к металлу, расположенному выше него, и катодом по отношению ко всем расположенным ниже. Это значит, что в судовых условиях, при наличии контакта стальных конструкций с конструкциями, изготовленными из алюминия, алюминиевомагние-вых и других сплавов, обязательно будут наблюдаться разрушения последних. По этой же причине на судне происходит сильное разрушение стального вала, на котором укреплен бронзовый или латунный гребной винт, рулей, расположенных вблизи винта и т. д.
Технические металлы, используемые для постройки судов, всегда бывают неоднородными, что связано с химическим составом металла, термической и механической обработкой, которым он „подвергался при изготовлении судна. Помимо структуры материала, на коррозию листов обшивки корпуса значительное влияние оказывает оставшаяся прокатная окалина, образовавшаяся при горячей прокатке металла. Обладая положительным потенциалом, она способствует очень интенсивной коррозии металла.
Окалина имеет сложное, слоистое строение и в зависимости от температуры прокатки листов может состоять из трех (FeO, Fe304 и Fe203), двух (FeO, Fe304 или Fe203) или одного (FeO или Fe304) слоя. Схематическое изображение многослойной окалины на малоуглеродистой стали представлено на рис. 11.
Неоднородность металлов является причиной того, что при наличии электролита на их поверхности образуются многоэлектродные гальванические элементы. При этом одни участки анодного характера будут сильно разрушаться, на других катодных участках будет выделяться водород или окислы металлов. На рис. 12 показана схема коррозии стального листа с частично сохранившейся окалиной. В прианодной зоне происходит интенсивное разъедание металла, на прокатной окалине выделяются гидроокисные соединения железа. Наличие неудаленной окалины может в 30—40 раз увеличить обычную для морских условий скорость коррозии металла. Особенное усиление коррозии при наличии окалины наблюдается на корпусе вблизи ватерлинии, что объясняется более легким доступом кислорода воздуха к этому району судна.

Рис. 3. Нормальный ряд напряжений
При постройке судна неизбежно использование конструкций, в которых встречается сочетание различных металлов. В этом случае электрохимическая коррозия имеет особенно интенсивный характер, сопровождаясь быстрым разрушением металла с более высоким электроотрицательным потенциалом. Поэтому алюминий, который благодаря свойству самопассивирования становится устойчивым во многих средах, теряет это свойство при контакте и подвергается сильной коррозии. Попадание морской воды, хлориды которой разрушают пассивную пленку, усиливает процесс коррозии.
Установлено, что алюминиевые сплавы, хотя и в меньшей степени, чем железные, чувствительны к периодическому смачиванию. Скорость коррозии конструкций, при периодическом смачивании в 7—12 раз выше, чем при постоянном погружении в морскую воду. Поэтому для защиты от коррозии конструкций из разнородных металлов необходимо принимать специальные меры: окраску по усиленной схеме и установку протекторов.
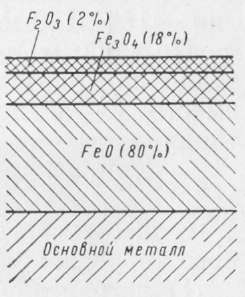
Рис. 4. Схема строения окалины на малоуглеродистой стали
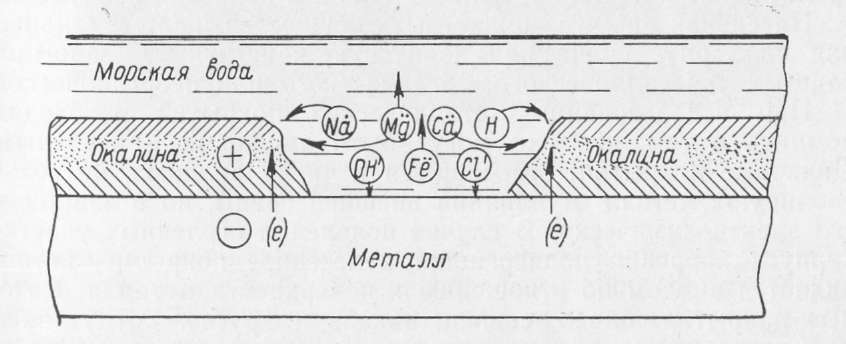
Рис. 5. Схема коррозионного процесса на стали при наличии частично разрушенной прокатной окалины
Об экономическом ущербе, причиняемом коррозией, можно судить по нижеприведенным данным. В США ежегодно сумма убытков, причиняемых коррозией всему хозяйству страны, оценивается в 6 млрд. долларов, в ФРГ — 2 млрд. марок, в Италии— 150—170 млрд. лир и т. д.
По данным Морского Регистра СССР имеются случаи, когда судно приходится капитально ремонтировать после 10—15 лет вместо 30—35 лет, на которые была рассчитана его эксплуатация.